Сімпоні розчин д/ін., 100 мг/мл по 0,5 мл у поперед. запов. руч. №1 з автоін`єкт.
Бакстер Фармасьютикал/Сілаг АГ для "Джонсон & Джонсон, ТОВ", США/Швейцарія-
Сімпоні р-н д/ін. 50 мг/0,5 мл ручка №3
Сілаг АГ для "Джонсон & Джонсон", Швейцарія/Російська Федерація -
Сімпоні р-н д/ін. 50 мг/0,5 мл ручка №1
Сілаг АГ для "Джонсон & Джонсон", Швейцарія/Російська Федерація -
Сімпоні р-н д/ін. 50 мг/0,5 мл шприц №1
Сілаг АГ для "Джонсон & Джонсон", Швейцарія/Російська Федерація -
Сімпоні р-н д/ін. 50 мг/0,5 мл шприц №3
Сілаг АГ для "Джонсон & Джонсон", Швейцарія/Російська Федерація -
Сімпоні розчин д/ін., 100 мг/мл по 0,5 мл у поперед. запов. шпр. №1 з пристр. UltraSafe
Сілаг АГ для "Джонсон & Джонсон", Швейцарія/Російська Федерація -
Сімпоні розчин д/ін., 100 мг/мл по 1 мл у поперед. запов. шпр. №1 з пристр. UltraSafe
Сілаг АГ для "Джонсон & Джонсон", Швейцарія/Російська Федерація -
Сімпоні розчин д/ін., 100 мг/мл по 1 мл у поперед. запов. руч. №1з автоін`єкт.
Сілаг АГ для "Джонсон & Джонсон", Швейцарія/Російська Федерація
Склад
діюча речовина: golimumab;
1 попередньо наповнений шприц або 1 попередньо наповнена ручка містить: голімумабу 50 мг в 0,5 мл;
допоміжні речовини: сорбітол (E 420), L–гістидин, L–гістидину моногідрохлориду моногідрат, полісорбат 80, вода для ін’єкцій.
Лікарська форма
Розчин для ін’єкцій.
Основні фізико-хімічні властивості: прозорий або злегка опалесцюючий, безбарвний або світло-жовтий розчин, який може містити невелику кількість прозорих або білих білкових частинок, що допустимо для розчинів, що містять білок.
Фармакотерапевтична група
Інгібітори фактору некрозу пухлин альфа (TNF?α).
Код АТХ L04AB06.
Імунологічні і біологічні властивості.
Фармакодинаміка.
Механізм дії
Голімумаб є людським моноклональним антитілом, яке формує високоафінні стабільні комплекси з розчинними та трансмембранними біоактивними формами фактору некрозу пухлин альфа (TNF-α) людини, що попереджує зв’язування TNF-α з власними рецепторами.
Зв’язування людського TNF з голімумабом призводить до нейтралізації TNF-α індукованої експресії на поверхні клітин молекул адгезії Е-селектину, молекули адгезії судинного ендотелію 1 типу (VCAM-1) та молекул міжклітинної адгезії (ICAM-1) ендотеліальними клітинами людини. In vitro, TNF - індукована секреція інтерлейкіну - 6 (IL-6), інтерлейкіну - 8 (IL-8) та гранулоцито-макрофаго-колонієстимулюючого фактору (GM-CSF) ендотеліальними клітинами людини також інгібувалася голімумабом.
На фоні терапії СІМПОНІ® відмічалося зменшення рівня С-реактивного білка (CRP) в порівнянні з групами плацебо, що призводило до значного зменшення в сироватці крові рівня IL-6, ICAM-1, матриксної металопротеїнази-3 (MMP-3) та фактору росту ендотелію судин (VEGF), у порівнянні з контрольною групою. Було продемонстровано зниження рівнів TNF у пацієнтів з ревматоїдним артритом та анкілозивним спондилітом, та рівнів IL-6 у пацієнтів з псоріатичним артритом. Ці зміни спостерігалися при першому обстеженні після введення першої дози препарату СІМПОНІ® (4-й тиждень) і зберігалися до 24 тижня.
Імуногенність
Антитіла до голімумабу були виявлені у 5 % пацієнтів з ревматоїдним артритом, псоріатичним артритом і анкілозивним спондилітом, які отримували препарат СІМПОНІ® протягом 52 тижнів у дослідженнях ІІІ фази. Майже всі антитіла нейтралізувалися in vitro. Частота утворення антитіл була зіставною у пацієнтів з різними ревматичними захворюваннями. У пацієнтів, які отримували супутню терапію метотрексатом, частота утворення антитіл була нижчою, ніж у пацієнтів, які приймали препарат СІМПОНІ® без метотрексату (3 % і 8 % відповідно).
Антитіла до голімумабу виявлялися у 3 % пацієнтів з виразковим колітом, які отримували голімумаб протягом 54 тижнів під час ІІ та ІІІ фази клінічних досліджень. У пацієнтів, які отримували супутню терапію імуномодуляторами (азатіоприном, 6-меркаптопурином та метотрексатом), частота утворення антитіл до голімумабу була нижчою, ніж у пацієнтів, які приймали препарат СІМПОНІ® без імуномодуляторів (1 % і 3 % відповідно).
Присутність антитіл до голімумабу може збільшувати ризик розвитку реакцій у місці ін’єкції. Невелика кількість пацієнтів з антитілами до голімумабу не дозволяє точно оцінити зв’язок між імуногенністю та клінічною ефективністю або безпекою.
Оскільки аналіз імуногенності є продукт- і метод-специфічним, порівняння рівня антитіл при лікуванні іншими препаратами не є коректним.
Фармакокінетика
Всмоктування. Після одноразового підшкірного введення голімумабу здоровим добровольцям або пацієнтам з ревматоїдним артритом середній час досягнення максимальної концентрації (Tmax) у сироватці крові становив від 2 до 6 днів. Після підшкірного введення 50 мг голімумабу здоровим добровольцям Cmax становила 3,1 ± 1,4 мкг/мл (середнє ± стандартне відхилення).
Всмоктування голімумабу було подібним після одноразового підшкірного введення в дозі 100 мг в область плеча, живота і стегна, а середня абсолютна біодоступність дорівнювала 51 %. Враховуючи практично пропорційну дозі фармакокінетику голімумабу після підшкірного введення, абсолютна біодоступність голімумабу в дозі 50 мг або 200 мг повинна бути подібною.
Розподіл. Після одноразового внутрішньовенного введення препарату середній об’єм розподілу становив 115 ± 19 мл/кг.
Виведення. Системний кліренс голімумабу складав 6,9 ± 2,0 мл/день/кг. Кінцевий період напіввиведення у здорових добровольців і пацієнтів з ревматоїдним артритом, псоріатичним артритом, анкілозивним спондилітом або виразковим колітом був подібним і складав 12 ± 3 днів.
У пацієнтів з ревматоїдним артритом, псоріатичним артритом або анкілозивним спондилітом, які отримували підшкірне введення голімумабу в дозі 50 мг кожні 4 тижні, сироваткові концентрації досягали рівноважного стану до 12 тижня. При одночасному застосуванні метотрексату з голімумабом підшкірно в дозі 50 мг кожні 4 тижні середня мінімальна залишкова концентрація в рівноважному стані складала 0,6 ± 0,4 мкг/мл
(± стандартне відхилення) у пацієнтів з активним ревматоїдним артритом, незважаючи на терапію метотрексатом, приблизно 0,5 ± 0,4 мкг/мл у пацієнтів з активним псоріатичним артритом і близько 0,8 ± 0,4 мкг/мл у пацієнтів з анкілозивним спондилітом. У пацієнтів з ревматоїдним артритом, псоріатичним артритом або анкілозивним спондилітом, які не отримували супутню терапію метотрексатом, мінімальна залишкова концентрація голімумабу в рівноважному стані була приблизно на 30 % нижче, ніж у пацієнтів, які отримували голімумаб з метотрексатом. У обмеженої кількості пацієнтів з ревматоїдним артритом, які отримували лікування голімумабом підшкірно протягом 6-місячного періоду, одночасне застосування метотрексату знижувало уявний кліренс голімумабу на 36 %. Однак, при популяційному фармакокінетичному аналізі було показано, що поєднане застосування NSAID, пероральних кортикостероїдів або сульфасалазину не впливає на удаваний кліренс голімумабу.
Після введення індукційних доз 200 мг та 100 мг голімумабу на 0 та 2 тижні відповідно, та надалі підтримуючих доз 50 мг та 100 мг підшкірно кожні 4 тижні пацієнтам з виразковим колітом, сироваткові концентрації голімумабу досягали рівноважного стану приблизно на 14 тижні після початку терапії. При застосуванні 50 мг або 100 мг голімумабу підшкірно кожні 4 тижні рівноважна залишкова концентрація у сироватці крові становила 0,9 ± 0,5 мкг/мл та 1,8 ± 1,1 мкг/мл відповідно.
У пацієнтів з виразковим колітом, яким застосовували дози 50 мг та 100 мг голімумабу підшкірно кожні 4 тижні, одночасне застосування імуномодуляторів не мало значного впливу на рівноважні концентрації голімумабу.
Поява антитіл до голімумабу зазвичай супроводжувалася зниженням мінімальної залишкової концентрації в рівноважному стані.
Лінійність. У пацієнтів з ревматоїдним артритом фармакокінетика голімумабу була пропорційною дозі в діапазоні від 0,1 до 10,0 мг/кг після одноразового внутрішньовенного введення. Після одноразового підшкірного введення здоровим добровольцям доз у діапазоні від 50 мг до 400 мг спостерігалася дозопропорційна фармакокінетика.
Вплив ваги на фармакокінетику. При популяційному фармакокінетичному аналізі виявлена тенденція до збільшення уявного кліренсу голімумабу при підвищенні маси тіла.
Показання Сімпоні розчин д/ін., 100 мг/мл по 0,5 мл у поперед. запов. руч. №1 з автоін`єкт.
Ревматоїдний артрит
СІМПОНІ® у комбінації з метотрексатом показаний для:
лікування ревматоїдного артриту в активній формі, від середнього до тяжкого ступеня у дорослих, у яких відмічається незадовільна відповідь на терапію DMARD, в тому числі метотрексатом.
лікування тяжкого, активного та прогресуючого ревматоїдного артриту у дорослих, які раніше не отримували терапію метотрексатом.
Було продемонстровано, що СІМПОНІ® в комбінації з метотрексатом зменшує частоту прогресування пошкодження суглобів за даними рентгенографії, а також покращує їх функціонування.
Псоріатичний артрит
СІМПОНІ®, у якості монотерапії або у комбінації з метотрексатом, показаний для лікування активного та прогресуючого псоріатичного артриту у дорослих, у яких раніше відмічалася незадовільна відповідь на терапію DMARD. СІМПОНІ® знижує частоту прогресування патології периферичних суглобів, що було продемонстровано за допомогою рентгенографії у пацієнтів, що мають підтипи захворювання із симетричним ураженням більшості суглобів, а також покращує фізичне функціонування.
Анкілозивний спондиліт
СІМПОНІ® показаний для лікування тяжкого активного анкілозивного спондиліту у дорослих, у яких раніше відмічалася незадовільна відповідь на традиційну терапію.
Виразковий коліт
СІМПОНІ® показаний для лікування активної форми виразкового коліту середнього або тяжкого ступеня у дорослих, у яких відмічається незадовільна відповідь на традиційну терапію, включаючи кортикостероїди, 6-меркаптопурин (6-МП) або азатіоприн (АЗА), або при непереносимості чи медичних протипоказаннях до застосування даних видів терапії.
Протипоказання Сімпоні розчин д/ін., 100 мг/мл по 0,5 мл у поперед. запов. руч. №1 з автоін`єкт.
Підвищена чутливість до голімумабу або до інших компонентів лікарського засобу. Туберкульоз в активній формі або інші тяжкі інфекції, такі як сепсис та опортуністичні інфекції.
Помірна або тяжка серцева недостатність (класу ІІІ/ІV за NYHA).
Взаємодія з іншими лікарськими засобами та інші види взаємодій.
Дослідження взаємодії не проводилися.
Одночасне застосування з іншими біологічними лікарськими засобами
Одночасне застосування з іншими біологічними лікарськими засобами для лікування тих самих захворювань, для лікування яких застосовується СІМПОНІ®, включаючи анакінру та абатацепт, не рекомендується (див. розділ «Особливості застосування»).
Живі вакцини/терапевтичні інфекційні речовини
Одночасне застосування живих вакцин або терапії іншими збудниками інфекцій із СІМПОНІ® не рекомендоване (див. розділи «Особливості застосування» та «Застосування у період вагітності або годування груддю»).
Метотрексат
Незважаючи на те, що супутнє застосування метотрексату призводить до більш високих рівноважних мінімальних концентрацій СІМПОНІ® у пацієнтів з ревматоїдним артритом, псоріатичним артритом і анкілозивним спондилітом, ці дані не свідчать про необхідність корекції дози СІМПОНІ® або метотрексату (див. розділ «Фармакокінетика»).
Особливості застосування.
Інфекції
Пацієнтів потрібно ретельно обстежувати на інфекції, включаючи туберкульоз, до, під час та після лікування СІМПОНІ®. Оскільки виведення голімумабу може тривати до 5 місяців, моніторинг необхідно продовжувати протягом цього періоду. Подальше лікування СІМПОНІ® потрібно зупинити у випадку розвитку серйозної інфекції або сепсису (див. розділ «Протипоказання»).
Не слід проводити терапію СІМПОНІ® у пацієнтів з клінічно значущими активними формами інфекцій. Необхідно проявляти обережність при вирішенні питання про застосування СІМПОНІ® у пацієнтів з хронічними інфекціями або наявністю рецидивуючих інфекцій в анамнезі. Необхідно рекомендувати пацієнтам по можливості уникати впливу потенційних факторів ризику розвитку інфекцій.
Пацієнти, що приймають блокатори TNF, більшою мірою схильні до розвитку серйозних інфекцій. Повідомлялося про випадки бактеріальних (в т. ч. сепсис та пневмонію), мікобактеріальних (в т. ч. туберкульоз), інвазивних грибкових та опортуністичних інфекцій, включаючи летальні випадки, у пацієнтів, які отримували лікування СІМПОНІ®. Деякі з цих серйозних інфекцій відмічалися у пацієнтів, які отримували супутню імуносупресивну терапію, що, на фоні основного захворювання, могло підвищити схильність до розвитку інфекцій. Необхідно ретельно контролювати стан пацієнтів та проводити повну діагностичну оцінку при появі симптомів розвитку нової інфекції. Терапію СІМПОНІ® необхідно припинити при розвитку у пацієнта нової серйозної інфекції або сепсису, розпочати відповідну протимікробну чи протигрибкову терапію та проводити її до досягнення контролю захворювання. У пацієнтів, котрі проживали або подорожували до регіонів, у яких інвазивні грибкові інфекції (наприклад, гістоплазмоз, кокцидіоїдомікоз або бластомікоз) є ендемічними, слід ретельно оцінити співвідношення ризику та користі перед початком терапії СІМПОНІ ®.
Туберкульоз
Повідомлялося про випадки туберкульозу у пацієнтів, які отримували терапію СІМПОНІ®. В більшості випадків туберкульоз був позалегеневим, в локальній або дисемінованій формі.
Перед початком терапії СІМПОНІ® слід провести обстеження пацієнтів для виключення активних та неактивних (латентних) форм туберкульозу. Обстеження має включати детальний анамнез, у тому числі відомості про захворювання на туберкульоз у минулому, можливі контакти з хворими на туберкульоз та попередню та/або супутню імуносупресивну терапію. Обов’язковим є проведення всім пацієнтам до початку терапії шкірного туберкулінового тесту і рентгенографії грудної клітки. Слід враховувати, що у тяжких хворих та імуноскомпрометованих пацієнтів може бути отримана псевдонегативна туберкулінова проба.
У разі встановлення діагнозу активної форми туберкульозу починати терапію СІМПОНІ® не можна (див. розділ «Протипоказання»).
При підозрі на наявність латентної форми туберкульозу необхідно проконсультуватися з фтизіатром. У всіх ситуаціях, описаних нижче, необхідно ретельно оцінювати співвідношення користі/ризику терапії препаратом СІМПОНІ®.
Якщо встановлено діагноз неактивної (латентної) форми туберкульозу, перед початком терапії СІМПОНІ® необхідно провести специфічне протитуберкульозне лікування.
У пацієнтів з кількома або багатьма значними факторами ризику розвитку туберкульозу, а також негативними результатами тесту на латентну форму туберкульозу, необхідно розглянути питання про призначення протитуберкульозної терапії перед початком лікування СІМПОНІ®. Застосування протитуберкульозної терапії також необхідно розглянути перед початком лікування СІМПОНІ ® у пацієнтів, у яких раніше відзначалася латентна або активна форма туберкульозу і немає підтвердження про проведений повний та адекватний курс протитуберкульозного лікування.
Повідомлялося про випадки розвитку активної форми туберкульозу у пацієнтів, які отримували СІМПОНІ® під час та після проведення лікування латентної форми туберкульозу. За пацієнтами, які лікуються СІМПОНІ®, слід ретельно спостерігати на предмет ознак та симптомів активної форми туберкульозу, включно з пацієнтами, результати обстеження яких на латентну форму були негативними, а також пацієнтами, які проходять лікування латентної форми туберкульозу, або раніше проходили протитуберкульозне лікування.
Усіх пацієнтів слід попередити про необхідність консультації лікаря при появі ознак/симптомів, що нагадують туберкульоз (наприклад постійний кашель, зменшення маси тіла, субфебрилітет), під час або після лікування СІМПОНІ®.
Реактивація вірусу гепатиту B (HBV)
Є повідомлення про реактивацію гепатиту В у пацієнтів, які отримували терапію антагоністами TNF, включаючи СІМПОНІ®, та були хронічними носіями вірусу (тобто мали позитивну реакцію на поверхневий антиген вірусу). Деякі з випадків були летальними.
Перед початком лікування СІМПОНІ® необхідно провести обстеження на наявність вірусу гепатиту В. Пацієнтам з позитивними результатами аналізу на вірус гепатиту В рекомендовано звернутися до лікаря з досвідом лікування гепатиту В.
Носіям вірусу гепатиту В, які потребують терапії з використанням СІМПОНІ®, слід проводити ретельний моніторинг ознак та симптомів активного гепатиту В протягом періоду лікування та декількох місяців після його закінчення. Даних щодо лікування пацієнтів, які є носіями вірусу гепатиту В, із застосуванням антивірусної терапії у комбінації з TNF-антагоністом для запобігання реактивації вірусу гепатиту В, немає. Пацієнтам, у яких спостерігається реактивація вірусу гепатиту В, потрібно припинити лікування СІМПОНІ® та розпочати ефективну антивірусну та підтримувальну терапію.
Злоякісні новоутворення та лімфопроліферативні порушення
Потенційна роль терапії блокаторами TNF у розвитку злоякісних пухлин невідома. Згідно з наявними даними, не можна виключити ризик розвитку лімфом, лейкемії або інших злоякісних новоутворень у пацієнтів, які отримують терапію антагоністами TNF. Необхідно з обережністю приймати рішення щодо застосування TNF-блокуючої терапії пацієнтам з анамнезом злоякісного новоутворення або при вирішенні продовжувати терапію у пацієнтів, у яких розвинулися злоякісні новоутворення.
Злоякісні пухлини у дітей
При проведенні постмаркетингового спостереження застосування TNF-блокаторів, зафіксовані випадки злоякісних новоутворень, деякі з яких були летальними у дітей, підлітків та молодих людей (віком до 22 років), які приймали TNF-блокатори (терапію було розпочато у дітей віком ≤ 18 років). Приблизно половину випадків становили лімфоми. Інші випадки були пов’язані з різноманітними іншими злоякісними новоутвореннями, включаючи рідкісні злоякісні новоутворення, що пов’язані з імуносупресією. Роль TNF-блокаторів у розвитку злоякісних новоутворень не може бути виключена.
Лімфома і лейкемія
У контрольованих фазах клінічних досліджень всіх TNF-блокаторів, включаючи СІМПОНІ®, випадки лімфоми спостерігалися частіше серед пацієнтів, які отримували терапію блокаторами TNF у порівнянні з контрольною групою пацієнтів. У клінічних дослідженнях СІМПОНІ® IIb і III фази частота розвитку лімфом у пацієнтів, які отримували терапію СІМПОНІ®, була вищою, ніж очікувана частота в загальній популяції. У постмаркетинговому періоді відзначалися випадки лейкемії у пацієнтів, які отримували терапію антагоністами TNF. Існує підвищений ризик виникнення лімфоми та лейкемії у пацієнтів з ревматоїдним артритом, які страждають довготривалим, високоактивним запальним захворюванням, яке ускладнює проведення оцінки ризику.
У постмаркетинговому періоді повідомлялося про поодинокі випадки гепатолієнальної Т-клітинної лімфоми у пацієнтів, які отримували лікування TNF-блокаторами (див. розділ «Побічні реакції»). Цей рідкісний вид Т-клітинної лімфоми зазвичай має дуже агресивний перебіг з летальними наслідками. Більшість таких випадків виникали у підлітків та молодих чоловіків, які одночасно з СІМПОНІ® застосовували азатіоприн (АЗА) або 6-меркаптопурин (6-МП) для лікування запального захворювання кишечнику. Слід ретельно зважити усі ризики одночасного застосування АЗА та 6-МП з СІМПОНІ®. Не можна виключити ризику розвитку гепатолієнальної Т-клітинної лімфоми у пацієнтів, які лікуються TNF-блокаторами.
Інші злоякісні новоутворення
У контрольованих фазах клінічних досліджень СІМПОНІ®, в яких брали участь пацієнти з ревматоїдним артритом, псоріатичним артритом, анкілозивним спондилітом та виразковим колітом, частота розвитку злоякісних пухлин (крім лімфоми і немеланоматозних злоякісних пухлин шкіри), була подібною в групі терапії СІМПОНІ® і контрольній групі.
Дисплазія/карцинома товстої кишки
Невідомо, чи впливає лікування голімумабом на ризик розвитку дисплазії або раку товстої кишки. Усі пацієнти з виразковим колітом, що мають підвищений ризик дисплазії/раку кишечника (наприклад пацієнти з довготривалим виразковим колітом або первинним склерозуючим холангітом) або пацієнти з дисплазією чи раком товстої кишки в анамнезі, повинні регулярно проходити обстеження на предмет дисплазії перед початком та протягом терапії. Обстеження має включати колоноскопію та біопсію. Слід ретельно зважити усі ризики та переваги лікування СІМПОНІ®, а також необхідність продовжувати лікування пацієнтів, у яких на фоні терапії діагноз дисплазії товстої кишки встановлюється вперше.
У пошуковому клінічному дослідженні, в якому оцінювали застосування СІМПОНІ® пацієнтам з тяжкою персистуючою астмою, злоякісні пухлини частіше відзначалися у пацієнтів, які отримували терапію СІМПОНІ®, порівняно з пацієнтами з контрольної групи (див. розділ «Побічні реакції»). Значимість цих даних невідома.
У пошуковому клінічному дослідженні, у якому оцінювали застосування іншого блокатора TNF – інфліксимабу, у пацієнтів з помірними та важкими хронічними обструктивними захворюваннями легень (ХОЗЛ), злоякісні пухлини (особливо пухлини легень, голови і шиї) частіше відзначалися у пацієнтів, які отримували терапію інфліксимабом, порівняно з пацієнтами контрольної групи. У всіх пацієнтів в анамнезі відзначалося інтенсивне куріння. Таким чином, необхідно дотримуватися обережності при застосуванні будь-якого антагоніста TNF пацієнтам з ХОЗЛ, а також пацієнтам з підвищеним ризиком злоякісних пухлин через інтенсивне куріння.
Рак шкіри
Були отримані повідомлення про випадки меланоми у пацієнтів, що отримували терапію TNF-блокаторами, включаючи СІМПОНІ®. Пухлина Меркеля реєструвалася у пацієнтів, які отримували інші антагоністи TNF (див. розділ «Побічні реакції»). Пацієнтам рекомендовано періодично проводити обстеження шкіри, особливо при наявності факторів ризику розвитку раку шкіри.
Застійна серцева недостатність
На тлі терапії блокаторами TNF (включаючи СІМПОНІ®) відзначалися випадки декомпенсації застійної серцевої недостатності, а також нові випадки застійної серцевої недостатності. У клінічному дослідженні іншого антагоніста TNF відзначалися випадки декомпенсації застійної серцевої недостатності та підвищення смертності через застійну серцеву недостатність. Застосування СІМПОНІ® пацієнтам із застійною серцевою недостатністю не вивчалося. СІМПОНІ® необхідно застосовувати з обережністю у пацієнтів з легкою серцевою недостатністю (класу I/II NYHA). Необхідно ретельно спостерігати за станом пацієнтів та припинити терапію СІМПОНІ® при прогресуванні симптомів серцевої недостатності або їх первинному розвитку (див. розділ «Протипоказання»).
Неврологічні ефекти
Застосування блокаторів TNF, включаючи СІМПОНІ®, було асоційовано з появою або загостренням клінічних симптомів та/або радіографічними ознаками демієлінізуючих захворювань центральної нервової системи, включаючи розсіяний склероз і периферичні демієлінізуючі порушення. У пацієнтів з демієлінізуючими розладами, в тому числі в анамнезі, необхідно ретельно оцінити співвідношення користі і ризику терапії блокаторами TNF. При появі симптомів даних порушень необхідно вирішити питання про припинення терапії СІМПОНІ® (див. розділ «Побічні реакції»).
Хірургічні втручання
Є обмежений досвід застосування препарату пацієнтам, яким проводились хірургічні процедури, включаючи артропластику. Необхідно враховувати тривалий період напіввиведення голімумабу у випадку планування будь-яких хірургічних процедур. Пацієнтам, які потребують проведення хірургічної операції під час лікування препаратом, слід перебувати під ретельним контролем виникнення інфекцій.
Імуносупресія
Не виключена роль блокаторів TNF, включаючи СІМПОНІ®, у впливі на імунологічні механізми, що захищають від інфекцій та злоякісних пухлин, оскільки TNF є медіатором запалення і модулятором клітинної імунної відповіді.
Аутоімунні процеси
Відносний дефіцит TNFα, спричинений анти-TNF-терапією, може ініціювати розвиток аутоімунного процесу. Якщо у хворого виникають симптоми, що нагадують вовчаковий синдром, а також виявляються антитіла до двоспіральної ДНК, лікування треба припинити (див. розділ «Побічні реакції»).
Гематологічні реакції
Повідомлялося про випадки панцитопенії, лейкопенії, нейтропенії, апластичної анемії та тромбоцитопенії у пацієнтів, які отримували TNF-блокатори. У рідкісних випадках в клінічних дослідженнях на тлі терапії СІМПОНІ® відзначалася цитопенія, включаючи панцитопенію. Усі пацієнти повинні одразу звернутися за медичною допомогою при появі симптомів гематологічних порушень (наприклад, тривала лихоманка, утворення синців, кровотеча, блідість). Необхідно припинити застосування препарату пацієнтам із підтвердженими істотними гематологічними патологіями.
Одночасне застосування інгібітору TNF та анакінри
Спостерігалися серйозні інфекції та нейтропенія у ході клінічних випробувань при супутньому застосуванні анакінри та етанерсепту (інгібітору TNF), що не мало терапевтичних переваг порівняно з монотерапією етанерсептом. Враховуючи характер небажаних реакцій, які спостерігалися на фоні такої комбінованої терапії, подібні токсичні ефекти можуть спостерігатися при застосуванні анакінри у комбінації з іншими блокаторами TNF. Тому не рекомендується застосовувати СІМПОНІ® у комбінації з анакінрою.
Одночасне застосування інгібітору TNF та абатацепту
У ході клінічних випробувань супутнє застосування TNF-блокуючих агентів та абатацепту асоціювалося з підвищенням ризику виникнення інфекцій, включаючи тяжкі інфекції, порівняно з монотерапією TNF-блокуючими агентами, без підвищення клінічної користі. Не рекомендується застосовувати СІМПОНІ® в комбінації з абатацептом.
Одночасне застосування з іншими біологічними лікарськими засобами
Інформації щодо одночасного застосування голімумабу з іншими біологічними лікарськими засобами, які використовують для лікування тих самих станів, що і голімумаб, недостатньо. Не рекомендовано застосовувати СІМПОНІ® одночасно з біологічними терапевтичними лікарськими засобами через можливість підвищення ризику виникнення інфекції та інших потенційних фармакологічних взаємодій.
Перехід з одного біологічного базисного модифікуючого протиревматичного препарату на інший
Під час переходу з одного біологічного препарату на інший слід ретельно спостерігати за клінічним станом пацієнта, оскільки перехресна біологічна активність може підвищувати ризик побічних реакцій, включаючи інфекції.
Вакцинації/ терапія збудниками інфекцій
Пацієнти, які отримують терапію СІМПОНІ®, можуть проводити вакцинацію, за винятком вакцинації живими вакцинами (див. розділи «Взаємодія з іншими лікарськими засобами та інші види взаємодій» та «Застосування у період вагітності або годування груддю»). Доступні лише обмежені дані результатів вакцинації або вторинного інфікування живими вакцинами пацієнтів, що отримують анти-TNF-терапію. Використання живих вакцин може призвести до клінічних проявів інфекцій, включаючи дисеміновані. Застосування терапії іншими збудниками інфекцій, такими як живі ослаблені бактерії (наприклад, інстиляції сечового міхура БЦЖ для лікування раку) може призвести до клінічних проявів інфекцій, включаючи дисеміновані. Не рекомендується призначати терапію збудниками інфекції одночасно з СІМПОНІ®.
Алергічні реакції
З досвіду післяреєстраційного застосування, після введення СІМПОНІ® відзначалися випадки серйозних системних реакцій гіперчутливості (включаючи анафілактичні реакції). Деякі з цих реакцій відзначалися після першого введення СІМПОНІ®. При розвитку анафілактичної реакції або інших серйозних алергічних реакцій необхідно негайно припинити терапію СІМПОНІ® і розпочати відповідне лікування.
Чутливість до латексу
Ковпачок голки ручки для ін’єкцій виготовлено з сухого натурального каучуку, що містить латекс, і може викликати алергічні реакції в осіб, чутливих до латексу.
Особливості застосування у деяких категорій пацієнтів.
Пацієнти похилого віку (≥ 65 років)
У дослідженнях ІІІ фази, у яких брали участь пацієнти з ревматоїдним артритом, псоріатичним артритом, анкілозивним спондилітом та виразковим колітом, не було відмінностей у небажаних реакціях, серйозних небажаних реакціях та серйозних інфекціях між пацієнтами у віці 65 років і старше, які отримували лікування препаратом СІМПОНІ®, та молодшими пацієнтами. Однак, слід бути обережними при лікуванні пацієнтів похилого віку та приділяти увагу можливості розвитку інфекції.
Пацієнти з порушеннями функції нирок і печінки
У пацієнтів з порушеннями функції нирок або печінки специфічних досліджень СІМПОНІ® не проводилося. У пацієнтів з порушенням функції печінки СІМПОНІ® необхідно застосовувати з обережністю (див. розділ «Спосіб застосування та дози»).
Пацієнти з непереносимістю фруктози
СІМПОНІ® містить сорбітол (E 420). Пацієнти з рідкісними спадковими порушеннями, пов’язаними з непереносимістю фруктози, не повинні приймати СІМПОНІ®.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами.
СІМПОНІ® може мати незначний вплив на швидкість реакції при керуванні автотранспортом та при роботі з іншими механізмами. Після застосування СІМПОНІ® може виникати запаморочення (див. розділ «Побічні реакції»).
Спосіб застосування та дози Сімпоні розчин д/ін., 100 мг/мл по 0,5 мл у поперед. запов. руч. №1 з автоін`єкт.
Терапію СІМПОНІ® необхідно розпочинати та проводити під наглядом кваліфікованих лікарів, які мають досвід діагностики та лікування ревматоїдного артриту, псоріатичного артриту, анкілозивного спондиліту або виразкового коліту.
Дозування
Ревматоїдний артрит. Призначають по 50 мг шляхом підшкірної ін’єкції один раз на місяць, в один і той же день місяця. СІМПОНІ® необхідно застосовувати в комбінації з метотрексатом.
Псоріатичний артрит. Призначають по 50 мг шляхом підшкірної ін’єкції один раз на місяць, в один і той же день місяця.
Анкілозивний спондиліт. Призначають по 50 мг шляхом підшкірної ін’єкції один раз на місяць, в один і той же день місяця.
Згідно з наявними даними для усіх вищезазначених показань, клінічна відповідь зазвичай досягається на 12-14 тижнях лікування (після введення 3-4 доз препарату). Необхідно розглянути питання про доцільність продовження терапії у пацієнтів, у яких відсутній терапевтичний ефект протягом вказаного періоду лікування.
Пацієнти з масою тіла більше 100 кг
Для усіх вищезазначених показань у пацієнтів з масою тіла більше 100 кг, у яких не було досягнуто позитивної клінічної відповіді після введення 3-4 доз препарату, може бути розглянуто питання про підвищення дози голімумабу до 100 мг 1 раз на місяць. При цьому необхідно врахувати підвищення ризику небажаних реакцій на лікарський препарат при застосування в дозі 100 мг, порівняно з дозою 50 мг. Якщо після введення 3-4 додаткових доз препарату (по 100 мг) не відмічається позитивного терапевтичного ефекту, слід розглянути доцільність продовження терапії у таких пацієнтів.
Виразковий коліт.
Пацієнти з масою тіла менше 80 кг
Призначають початкову дозу 200 мг, наступну 100 мг на тижні 2, потім по 50 мг кожні 4 тижні.
Пацієнти з масою тіла 80 кг або більше
Призначають початкову дозу 200 мг, наступну 100 мг на тижні 2, потім по 100 мг кожні 4 тижні.
Протягом підтримуючого лікування можна поступово знижувати дозу кортикостероїдів згідно з клінічними рекомендаціями.
Доступні дані демонструють, що клінічна відповідь зазвичай досягається на 12-14 тижнях лікування (після введення 4 доз). Необхідно розглянути питання про доцільність продовження терапії у пацієнтів, у яких відсутній терапевтичний ефект протягом вказаного періоду лікування.
Пропуск введення препарату.
Якщо пацієнт пропустив чергове введення СІМПОНІ® в запланований день, то пропущену дозу слід ввести відразу після того, як пацієнт згадав про це. Не потрібно вводити подвійну дозу препарату, щоб компенсувати пропуск дози. Введення наступної дози має бути проведено згідно з вказівками нижче:
- якщо після пропуску введення препарату пройшло менше 2 тижнів, то пацієнт повинен ввести пропущену дозу препарату та надалі дотримуватися попереднього графіку введення препарату;
- якщо після пропуску введення препарату пройшло більше 2 тижнів, то пацієнт повинен ввести пропущену дозу препарату та надалі дотримуватись нового щомісячного графіку, починаючи з дати цієї ін’єкції.
Пацієнти похилого віку ( ≥ 65 років).
Корекція дози пацієнтам похилого віку не потрібна.
Пацієнти з порушенням функції нирок та/або печінки.
Дослідження препарату у пацієнтів цієї групи не проводилося. Рекомендації відносно дозування препарату відсутні.
Спосіб застосування
Для підшкірного введення. За рішенням лікаря та після проведення навчання методики підшкірних ін’єкцій, пацієнти можуть самостійно вводити СІМПОНІ® з наступним контролем лікаря за необхідності. Пацієнтів слід проінструктувати щодо необхідності введення препарату в повному об’ємі та у відповідності до детальної інструкції з техніки введення.
Інструкція із самостійного введення СІМПОНІ®.
Якщо пацієнт хоче проводити ін’єкції самостійно, з ним повинен провести тренування медичний персонал щодо підготовки ін’єкції та її проведення. Якщо тренування не проведено, слід звернутися до лікаря.
Попередньо наповнена ручка з автоін?єктором.
1. Підготовка ручки до використання.
- Не струшуйте ручку для ін’єкцій.
- Не знімайте захисну кришку ручки, доки це не буде вказано в інструкції.
Перевірте термін придатності, вказаний на ручці (або коробці). Наведений термін трактується як останній день вказаного місяця та року. Якщо термін придатності минув, не можна використовувати ручку для ін’єкцій.
Перевірте захисну кришку ручки. Не використовуйте лікарський засіб у разі пошкодження наклейки контролю першого відкриття.
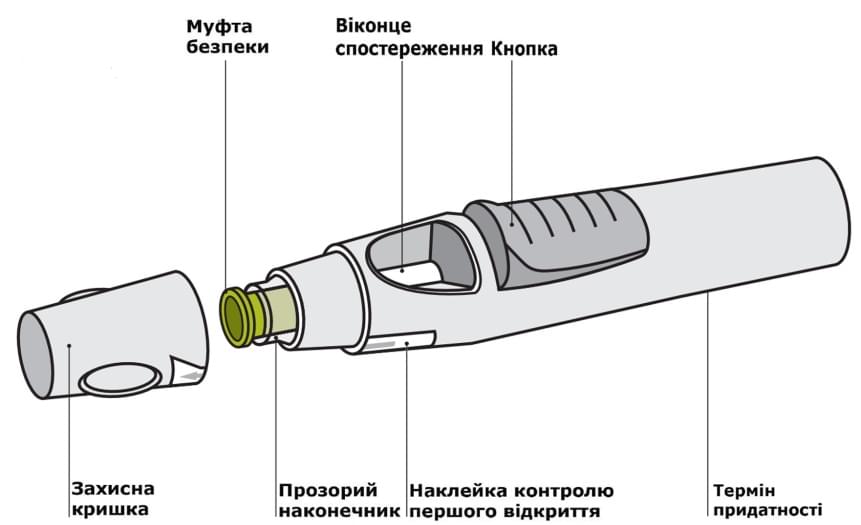
Зачекайте 30 хвилин для нагріву ручки до кімнатної температури. Перед застосуванням препарату слід дістати його з холодильника та коробки, та залишити ручку для ін’єкцій на 30 хвилин при кімнатній температурі у недоступному для дітей місці. Не слід нагрівати ручку жодним чином (у мікрохвильовій печі, в гарячій воді). Кришку не знімати.
Підготовка іншого обладнання. Під час очікування нагріву ручки підготуйте всі інші засоби, що можуть вам знадобитися для проведення ін’єкції (ватний диск, дезінфікуючий розчин).
Перевірка розчину для ін’єкцій. Роздивіться розчин через віконце спостереження. Впевніться, що розчин на вигляд прозорий чи злегка опалесцюючий (має перламутровий блиск), безбарвний або світло-жовтого кольору. Рідина може містити невелику кількість прозорих або білих білкових частинок, що допустимо для розчинів, що містять білок. Ви можете помітити також бульбашку повітря всередині контейнера. Не використовуйте лікарський засіб, якщо рідина містить осад або інші тверді включення. У такому випадку зверніться до лікаря.
2. Вибір місця ін’єкції.
- Рекомендованим місцем для ін’єкції при самостійному введенні є передня середня частина стегна.
- Альтернативним місцем введення препарату є нижня частина живота, нижче пупка, за виключенням поверхні у 5 см безпосередньо під пупком.
- Не вводьте лікарський препарат у ділянки, де шкіра є ніжною, має синці, почервоніння, лущення, затвердіння, шрами або розтяжки.
Вибір місця ін’єкції за участі помічника. Якщо ін’єкцію проводить ваш помічник, можна також використати зовнішню поверхню верхньої частини плеча.
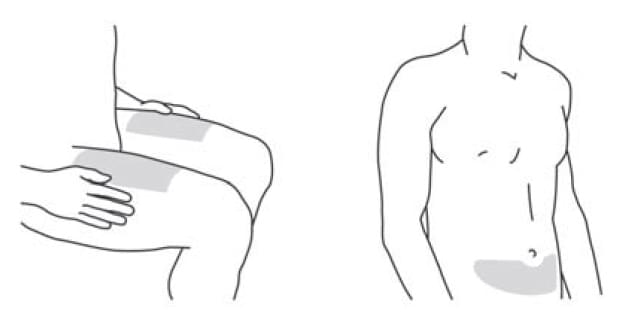
Всі вказані ділянки можуть бути використані для ін’єкції незалежно від типу та розміру тіла.
Підготування місця введення.
- Ретельно вимийте руки милом і теплою водою.
- Перед проведенням ін’єкції продезінфікуйте руки та протріть місце ін’єкції ватним диском, змоченим дезінфікуючим розчином (наприклад, спиртом).
- Залишіть місце ін’єкції до висихання перед введенням. Не дмухайте та не торкайтеся продезінфікованої ділянки шкіри.
3. Введення лікарського засобу.
Не слід знімати захисну кришку, доки ви не будете готові проводити ін’єкцію препарату. Ін’єкцію необхідно провести не більше ніж протягом 5 хвилин після видалення кришки.
Зняття захисної кришки. Після готовності до проведення ін’єкції, легко поверніть кришку для видалення наклейки контролю першого відкривання. Зніміть ковпачок та викиньте його.
Не слід повертати кришку на місце знову, оскільки це може пошкодити голку всередині ручки. Не використовуйте ручку, якщо вона впала після того, як кришка була знята.
Притисніть ручку до обраного місця введення.
Зручно візьміть ручку в руку. Не натискайте на кнопку в цей момент. Оберіть один з двох способів введення: рекомендований спосіб без защипування ділянки шкіри або, за бажанням, із защипуванням шкіри з метою створення більш твердої поверхні для ін’єкції. Не натискаючи на кнопку, легко притисніть відкритий кінець ручки до шкіри під прямим кутом (малюнок 3).
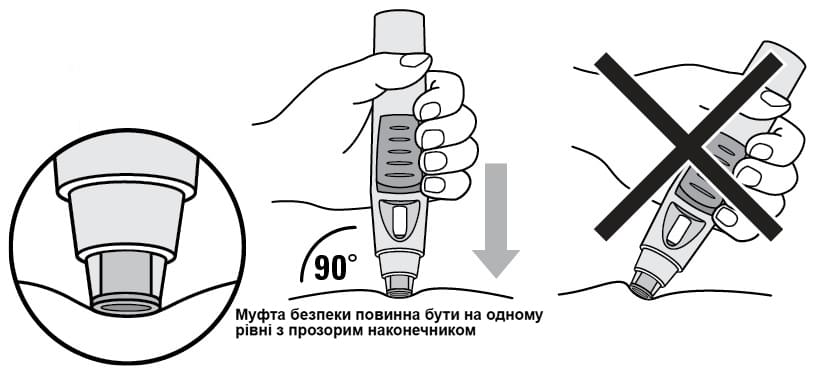
Малюнок 3
Натисніть кнопку для введення лікарського засобу (мал. 4).
Продовжуючи тримати ручку відповідним чином, натисніть на виступаючу частину кнопки. Ви не зможете натиснути на кнопку, якщо ручка розміщена невірно по відношенню до поверхні шкіри та поки муфта безпеки не зсунеться.
Після натискання кнопка залишиться в такому положенні, подальший тиск на кнопку можна припинити. Перше голосне «клацання» («клік») вказує на те, що голка введена та ін’єкцію розпочато. Укол голки ви можете не відчути.
Не слід підіймати ручку над шкірою. Якщо ви піднімете ручку, ви можете не отримати повну дозу препарату.
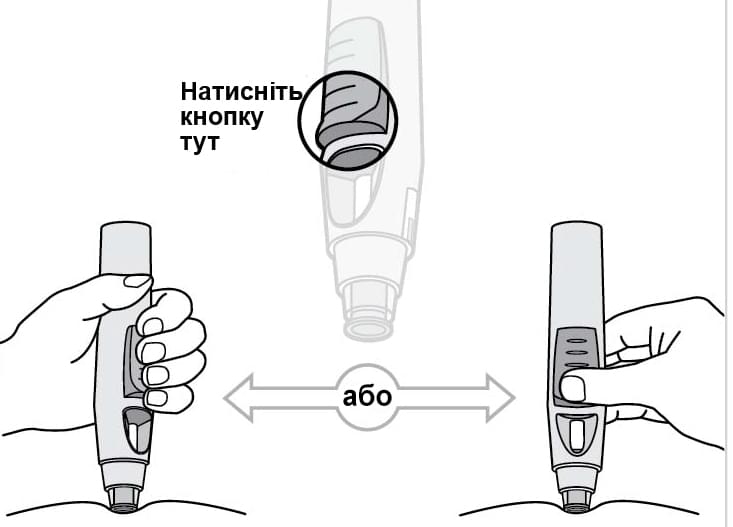
Малюнок 4
Продовжуйте тримати ручку на шкірі, доки не почуєте друге «клацання» («клік»).
Продовжуйте тримати ручку відповідним чином, поки не почуєте друге «клацання». Зазвичай введення дози лікарського засобу триває 3-6 секунд, але може зайняти до 15 секунд. Друге «клацання» («клік») означає, що ін’єкція закінчилась і голка повернулась до ручки. Підійміть ручку із місця ін’єкції.
Примітка: Якщо у вас є вади слуху, відрахуйте 15 секунд від моменту натискання на кнопку, а потім підійміть ручку із місця ін’єкції.
4. Після ін’єкції.
Використайте ватний диск або тампон. При необхідності просушіть місце ін’єкції за допомогою ватного диска або тампона від невеликої кількості крові або рідини з місця ведення та заклейте пластиром. Не тріть шкіру в місці ін’єкції.
Перевірте віконце спостереження. Після ін’єкції перевірте віконце спостереження та переконайтеся, що спостерігається жовтий індикатор. Якщо жовтий індикатор не спостерігається або якщо ви вважаєте, що не отримали ін’єкцію лікарського засобу, зверніться за допомогою до лікаря. Не вводьте другу дозу без консультації із лікарем.
Відразу ж після використання необхідно викинути ручку до контейнера зі сміттям. Викиньте ручку в контейнер відразу після проведення ін’єкції.
Якщо ви відчуваєте, що щось пішло не так із системою введення, або якщо ви не впевнені, зверніться до свого лікаря.
Попередньо наповнений шприц з пристроєм UltraSafe.
1. Підготовка шприца до використання.
Тримайте попередньо наповнений шприц ВИКЛЮЧНО за корпус.
Не слід:
- тримати шприц за будь-які інші частини окрім корпусу;
- відтягувати поршень назад;
- струшувати попередньо наповнений шприц;
- завчасно знімати захисний ковпачок з голки;
- торкатися затискача активації запобіжника голки (позначені * на схематичному зображенні шприца) для попередження передчасного закриття голки запобіжником.
Перевірте термін придатності, вказаний на шприці, дивлячись крізь віконце спостереження. Якщо ви не бачите термін придатності, візьміть шприц за корпус та поверніть ковпачок голки до появи терміну придатності у віконці спостереження. Термін придатності також наведено на зовнішній картонній коробці. Наведений термін трактується як останній день вказаного місяця та року. Якщо термін придатності минув, не можна використовувати шприц для ін’єкцій.
Зачекайте 30 хвилин для нагріву шприца до кімнатної температури. Перед застосуванням препарату слід дістати його з холодильника та коробки, та залишити шприц для ін’єкцій на 30 хвилин при кімнатній температурі у недоступному для дітей місці. Не слід нагрівати шприц жодним чином (у мікрохвильовій печі, в гарячій воді). Захисний ковпачок не знімати.
Підготовка іншого обладнання. Під час очікування нагріву шприца підготуйте всі інші засоби, що можуть вам знадобитися для проведення ін’єкції (ватний диск, дезінфікуючий розчин).
Перевірка розчину для ін’єкцій. Роздивіться розчин через віконце спостереження. Впевніться, що розчин на вигляд прозорий чи злегка опалесцюючий (має перламутровий блиск), безбарвний або світло-жовтого кольору. Рідина може містити невелику кількість прозорих або білих білкових частинок, що допустимо для розчинів, що містять білок. Не використовуйте лікарський засіб, якщо рідина містить осад або інші тверді включення. У такому випадку зверніться до лікаря.
2. Вибір місця ін’єкції.
- Рекомендованим місцем для ін’єкції при самостійному введенні є передня середня частина стегна.
- Альтернативним місцем введення препарату є нижня частина живота, нижче пупка, за виключенням поверхні у 5 см безпосередньо під пупком.
- Не вводьте лікарський препарат у ділянки, де шкіра є ніжною, має синці, почервоніння, лущення, затвердіння, шрами або розтяжки.
Вибір місця ін’єкції за участі помічника. Якщо ін’єкцію проводить ваш помічник, можна також використати зовнішню поверхню верхньої частини плеча.

Всі вказані ділянки можуть бути використані для ін’єкції незалежно від типу та розміру тіла.
Підготування місця введення.
- Ретельно вимийте руки милом і теплою водою.
- Перед проведенням ін’єкції продезінфікуйте руки та протріть місце ін’єкції ватним диском, змоченим дезінфікуючим розчином (наприклад, спиртом).
- Залишіть місце ін’єкції до висихання перед введенням. Не дмухайте та не торкайтеся продезінфікованої ділянки шкіри.
3. Введення лікарського засобу.
Не слід знімати захисний ковпачок, доки ви не будете готові проводити ін’єкцію препарату. Ін’єкцію необхідно провести не більше ніж протягом 5 хвилин після видалення ковпачка.
Зняття захисного ковпачка. Після готовності до проведення ін’єкції, тримайте корпус шприца однією рукою. Потягніть за ковпачок другою рукою та зніміть його. Не торкайтеся поршня голки під час зняття кришки.
Ви можете помітити бульбашку повітря всередині контейнера та краплю рідини на кінці голки, які не слід видаляти.
Введіть лікарський засіб якомога швидше після зняття захисного ковпачка.
Не торкайтеся голки та не допускайте її контакту з будь-якою іншою поверхнею. Не використовуйте попередньо наповнений шприц, якщо він упав після зняття ковпачка.
Розташування шприца для проведення ін’єкції. Візьміть попередньо наповнений шприц за корпус однією рукою між середнім та вказівним пальцями і розташуйте великий палець на верхівці головки поршня. Другою рукою обережно затисніть попередньо продезінфіковану поверхню шкіри в обраному для введення місці. Тримайте шприц обережно та не відтягуйте поршень до себе.
Введення лікарського засобу. Розташуйте голку під кутом приблизно 45 градусів до шкіри. Одним швидким рухом введіть голку у шкіру на всю її довжину.
Натискаючи на поршень, вводьте розчин лікарського засобу, доки головка поршня повністю не розташується між крилами запобіжника голки. Продовжуючи тиснути на головку поршня, вийміть голку та відпустіть ділянку шкіри.
Повільно зніміть великий палець з головки поршня; порожній шприц почне рухатись, доки вся голка не буде закрита запобіжником.
4. Після ін’єкції.
Використайте ватний диск або тампон. При необхідності, просушіть місце ін’єкції за допомогою ватного диска або тампона від невеликої кількості крові або рідини з місця ведення та заклейте пластиром. Не тріть шкіру в місці ін’єкції.
Відразу ж після використання необхідно викинути шприц до контейнера зі сміттям. Викиньте шприц в контейнер відразу після проведення ін’єкції. Не намагайтеся знову надіти на нього кришку.
В жодному разі не використовуйте шприц повторно. Якщо ви відчуваєте, що щось пішло не так із системою введення, або якщо ви не впевнені, зверніться до свого лікаря.
Діти.
Ефективність та безпека застосування СІМПОНІ® дітям не встановлена. Доступні дані відсутні.
Побічні реакції Сімпоні розчин д/ін., 100 мг/мл по 0,5 мл у поперед. запов. руч. №1 з автоін`єкт.
Профіль безпеки
Під час клінічних досліджень найчастішими побічними реакціями, про які повідомлялося, були інфекції верхніх дихальних шляхів. Найбільш серйозні небажані реакції включали серйозні інфекції (в тому числі сепсис, пневмонію, туберкульоз, інвазивні грибкові та опортуністичні інфекції), демієлінізуючі порушення, лімфому, реактивацію вірусу гепатиту В (HBV), застійну серцеву недостатність, аутоімунні процеси (вовчакоподібний синдром) та гематологічні реакції.
Побічні реакції, які спостерігалися в клінічних дослідженнях та про які повідомлялося під час післяреєстраційного застосування голімумабу, наведено нижче. В рамках зазначених класів систем та органів небажані реакції на лікарський препарат описані в залежності від частоти за наступним принципом: дуже часті (понад 10 %), часті (1-10 %), нечасті (0,1-1 %), поодинокі (0,01-0,1 %), рідкісні (менше 0,01 %) та невідомо (частота не може бути визначена з доступних даних). Всередині кожного класу частоти небажані реакції представлені у порядку зменшення серйозності.
Системи
Частота реакції
Характер реакції
Інфекції та інвазії
дуже часті
інфекції верхніх дихальних шляхів (назофарингіт, фарингіт, ларингіт та риніт)
часті
бактеріальні інфекції (целюліт), інфекція нижніх дихальних шляхів (пневмонія), вірусні інфекції (грип та герпес), бронхіт, синусит, поверхневі грибкові інфекції, абсцес
нечасті
сепсис включно із септичним шоком, опортуністичні інфекції (інвазивні грибкові інфекції [гістоплазмоз, кокцидіоїдомікоз, пневмоцистоз], бактеріальна, атипова мікобактеріальна інфекція і протозойна інфекція), бактеріальний артрит, пієлонефрит
поодинокі
реактивація вірусу гепатиту В, туберкульоз, інфекційний бурсит
Новоутворення доброякісні, злоякісні та не уточнені
нечасті
новоутворення (злоякісні пухлини шкіри, плоскоклітинна карцинома і меланоцитарний невус)
поодинокі
лімфома, лейкемія, меланома
невідомо
меркеліома*, гепатолієнальна Т-клітинна лімфома *
3 боку крові та
лімфатичної системи
часті
анемія
нечасті
лейкопенія, тромбоцитопенія, панцитопенія
поодинокі
апластична анемія*
3 боку імунної
системи
часті
алергічні реакції (бронхоспазм, гіперчутливість, кропив’янка), позитивна реакція на аутоантитіла
поодинокі
серйозні системні реакції гіперчутливості (включаючи анафілактичну реакцію), васкуліт (системний), саркоїдоз
Порушення з боку ендокринної системи
нечасті
порушення з боку щитовидної залози (гіпотиреоз, гіпертиреоз і зоб)
Порушення харчування та обміну речовин
нечасті
підвищення рівня глюкози крові, підвищення рівня ліпідів
Психічні порушення
часті
депресія, безсоння
Порушення з боку нервової системи
часті
запаморочення, головний біль, парестезія
нечасті
порушення рівноваги
поодинокі
демієлінізуючі порушення (центральні і периферичні), дизгевзія
Порушення з боку органів зору
нечасті
порушення зору (розмитість зору, зниження гостроти зору), кон’юнктивіт, алергічні захворювання очей (свербіж, подразнення)
Кардіологічні порушення
нечасті
аритмія, ішемічні порушення коронарних артерій
поодинокі
застійна серцева недостатність (поява або прогресування)
Порушення з боку судинної системи
часті
гіпертензія
нечасті
тромбоз (тромбоз глибоких вен, аорти), приливи
поодинокі
феномен Рейно
Респіраторні, торакальні та медіастинальні порушення
часті
астма і супутні симптоми (хрипи і гіперактивність бронхів)
нечасті
інтерстиціальна хвороба легенів
Порушення з боку травної системи
часті
диспепсія, біль в епігастральній області та в животі, нудота, запальні порушення шлунково-кишкового тракту (гастрит і коліт), стоматит
нечасті
закреп, гастроезофагеальна рефлюксна хвороба
Порушення з боку печінки
часті
підвищення рівня аланінамінотрансферази (АЛТ), підвищення рівня аспартатамінотраснферази (АСТ)
нечасті
холелітіаз, порушення з боку печінки
Порушення з боку шкіри та підшкірної клітковини
часті
свербіж, висип, алопеція, дерматит
нечасті
бульозні шкірні реакції, псоріаз (розвиток або прогресування існуючого, долонний/підошовний і пустульозний), кропив’янка
поодинокі
лущення шкіри, васкуліт (шкірний)
Порушення з боку кістково-м’язової системи та сполучної тканини
поодинокі
вовчакоподібний синдром
Порушення з боку сечовидільної системи та нирок
поодинокі
порушення з боку сечового міхура, порушення з боку нирок
Порушення з боку репродуктивної системи та молочної залози
нечасті
порушення з боку молочної залози, менструальні порушення
Системні порушення і ускладнення в місці введення
часті
лихоманка, астенія, реакції в місці ін’єкції (почервоніння в місці ін’єкції, кропив’янка, ущільнення, біль, синець, свербіж, подразнення і парестезія), дискомфорт у грудній клітці
поодинокі
уповільнене загоювання ран
Травми, отруєння та ускладнення процедури
часті
переломи кісток
* – спостерігалися на тлі застосування інших блокаторів TNF та не відзначалися в клінічних дослідженнях голімумабу.
Опис вибіркових побічних реакцій
Інфекції
Під час клінічних досліджень інфекції верхніх дихальних шляхів були найбільш частими побічними реакціями на лікарський засіб, про які повідомлялося у 12,6 % пацієнтів у групі голімумабу у порівнянні з 10,7 % у контрольній групі. У дослідженнях з періодом спостереження два роки, частота виникнення інфекцій верхніх дихальних шляхів становила 35,9 випадків на 100 пацієнто-років. Інфекції спостерігалися у 22,8 % пацієнтів, які отримували голімумаб у порівнянні з 19,9 % пацієнтів контрольної групи, серйозні інфекції спостерігалися у 1,4 % пацієнтів, які отримували лікування голімумабом та у 1,3 % контрольної групи. Під час досліджень індукції ремісії виразкового коліту серйозні інфекції спостерігалися у 0,8 % пацієнтів, які отримували голімумаб, у порівнянні з 1,5 % пацієнтів, які отримували плацебо. Тяжкі інфекції у пацієнтів, які отримували голімумаб, включали туберкульоз, бактеріальні інфекції включно з сепсисом та пневмонією, інвазивні грибкові інфекції та інші опортуністичні інфекції. Деякі випадки мали летальні наслідки. У дослідженнях з періодом спостереження 2 роки, серед пацієнтів, які отримували голімумаб у дозі 100 мг, спостерігалася вища частота виникнення тяжких інфекцій, включаючи опортуністичні інфекції та туберкульоз, ніж серед пацієнтів, які отримували голімумаб у дозі 50 мг.
Злоякісні новоутворення
Лімфома. Частота розвитку лімфом у пацієнтів, які отримували лікування голімумабом, за даними клінічних досліджень була більшою, ніж очікувана частота в загальній популяції. У дослідженні з наступним спостереженням протягом 2 років, частота виникнення лімфоми була вищою серед пацієнтів, які отримували голімумаб у дозі 100 мг, ніж серед пацієнтів, які отримували 50 мг голімумабу. Лімфому діагностували у 9 пацієнтів (у 1 пацієнта у групі 50 мг голімумабу та у 8 пацієнтів у групі 100 мг голімумабу). Більшість лімфом виникали під час дослідження за участю пацієнтів, які раніше отримували лікування інгібіторами TNF?α, з більшою тривалістю захворювання, а також з захворюванням, резистентним до лікування (див. розділ «Особливості застосування»).
Інші злоякісні новоутворення. У контрольованих фазах клінічних досліджень та за результатами подальшого спостереження протягом 2 років, частота розвитку злоякісних пухлин (крім лімфоми і немеланоматозних злоякісних пухлин шкіри), була подібною в групі терапії СІМПОНІ® і контрольній групі. За результатами подальшого спостереження протягом 2 років частота розвитку злоякісних пухлин (крім лімфоми і немеланоматозних злоякісних пухлин шкіри) була подібною до частоти у загальній популяції.
У дослідженнях з періодом спостереження 2 роки немеланоматозний рак шкіри діагностували у 5 пацієнтів, які отримували плацебо, 10 пацієнтів, які отримували голімумаб у дозі 50 мг та 29 пацієнтів, які отримували голімумаб у дозі 100 мг. Під час базисних досліджень з періодом спостереження 2 роки злоякісні пухлини, окрім лімфоми і немеланоматозних злоякісних пухлин шкіри, були діагностовані у 5 пацієнтів, які отримували плацебо, 20 пацієнтів, які отримували голімумаб у дозі 50 мг та 32 пацієнтів, які отримували голімумаб у дозі 100 мг (див. розділ «Особливості застосування»).
Побічні реакції під час клінічних досліджень у пацієнтів з астмою
У пошуковому клінічному дослідженні пацієнти з тяжкою персистуючою астмою отримували дозу насичення голімумабу (150 % звичайної терапевтичної дози) підшкірно на 0 тижні, надалі – 200 мг, 100 мг або 50 мг голімумабу через кожні 4 тижні протягом 52 тижнів терапії. Повідомлялося про 8 випадків злоякісних новоутворень у групі голімумабу та відсутність випадків у групі плацебо. Лімфома була діагностована у 1 пацієнта, немеланоматозна злоякісна пухлина шкіри – у 2 пацієнтів, у 5 пацієнтів – інші злоякісні новоутворення. Специфічного групування за типами злоякісних новоутворень не було.
Протягом плацебо-контрольованого дослідження частота виникнення злоякісних новоутворень усіх типів становила 3,19 на 100 пацієнто-років у групі голімумабу. У даному дослідженні частота лімфоми становила 0,40, немеланоматозного раку шкіри – 0,79 та інших злоякісних пухлин – 1,99 на 100 пацієнто-років у групі голімумабу. У групі плацебо частота злоякісних пухлин становила 0,00 на 100 пацієнто-років. Значимість цих даних невідома.
Неврологічні ефекти
У клінічних дослідженнях з наступним періодом спостереження протягом 2 років відмічалося збільшення частоти випадків демієлінізації у пацієнтів, що отримували голімумаб у дозі 100 мг у порівнянні з пацієнтами, що отримували 50 мг голімумабу (див. розділ «Особливості застосування»).
Підвищення рівнів печінкових ферментів
У клінічних дослідженнях ревматоїдного артриту та псоріатичного артриту незначні підвищення рівнів аланінамінотрансферази (АЛТ) (до 3х разів від верхньої межі норми) були подібними у пацієнтів з ревматоїдним артритом та псоріатичним артритом (22,1 % до 27,4 %). У дослідженні анкілозивного спондиліту незначне підвищення АЛТ спостерігалося у більшої кількості пацієнтів у групі голімумабу (25,6 %), ніж у групі плацебо (3,9 %). При проведенні досліджень ревматоїдного та псоріатичного артриту з наступним періодом спостереження протягом 5 років, частота підвищень рівня АЛТ була подібною у групах голімумабу в обох дослідженнях. У пацієнтів з анкілозивним спондилітом частота незначного підвищення рівня АЛТ була вищою у групі голімумабу, ніж у пацієнтів контрольної групи. У дослідженні індукції ремісії виразкового коліту незначне підвищення рівня АЛТ (до 3х разів від верхньої межі) спостерігалося майже в однакової кількості пацієнтів у групі голімумабу та контрольній групі (8,0 % та 6,9 % відповідно). У дослідженні підтримуючої терапії виразкового коліту з наступним періодом спостереження протягом 1 року частота незначного підвищення рівня АЛТ у пацієнтів, які отримували голімумаб, становила 17,4 %.
У дослідженнях ревматоїдного артриту та анкілозивного спондиліту підвищення рівня АЛТ більше ніж у 5 разів від верхньої межі норми спостерігалося нечасто, здебільшого у пацієнтів, які отримували голімумаб (0,4 % до 0,9 %) у порівнянні з пацієнтами контрольної групи (0,0 %). Такої залежності не спостерігалося серед пацієнтів з псоріатичним артритом. Під час досліджень ревматоїдного артриту, псоріатичного артриту та анкілозивного спондиліту з наступним періодом спостереження 5 років, частота підвищення рівня АЛТ більше ніж у 5 разів від верхньої межі норми була подібною у групі голімумабу та у контрольній групі. Загалом, такі підвищення рівня АЛТ були безсимптомними та знижувалися або нормалізувалися протягом лікування або після припинення лікування голімумабом, або при зміні лікарських засобів, які застосовувалися одночасно. У контрольованому дослідженні індукції ремісії виразкового коліту підвищення рівня АЛТ більше ніж у 5 разів від верхньої межі норми спостерігалося майже в однакової кількості пацієнтів у групі голімумабу та контрольній групі (0,3 % та 1,0 % відповідно). У дослідженні підтримуючої терапії виразкового коліту з періодом спостереження 1 рік підвищення рівня АЛТ більше ніж у 5 разів від верхньої межі спостерігалося у 0,7 % у пацієнтів, які отримували голімумаб.
Протягом базисних досліджень ревматоїдного артриту, псоріатичного артриту та анкілозивного спондиліту в одного пацієнта з існуючими порушеннями функції печінки та одночасним застосуванням інших лікарських засобів, який отримував голімумаб, розвинувся неінфекційний гепатит з жовтяницею з летальним наслідком. Роль голімумабу як сприяючого або загострюючого фактору не може бути виключена.
Реакції у місці введення
У контрольованих клінічних дослідженнях у групі пацієнтів, які отримували голімумаб, частота розвитку небажаних реакцій у місці введення відмічалася у 5,1 %, у порівнянні з 2,0 % в контрольній групі. Наявність антитіл до голімумабу може підвищувати ризик розвитку небажаних реакцій у місці введення. Більшість таких реакцій були від легкого до помірного ступеню тяжкості, найчастіше повідомлялося про появу почервоніння в місці ін’єкції. Реакції в місці введення зазвичай не призводили до відміни лікування препаратом.
У клінічних дослідженнях у пацієнтів з ревматоїдним артритом, псоріатичним артритом, анкілозивним спондилітом, тяжкою персистуючою астмою та у пацієнтів з виразковим колітом, у жодного пацієнта не виникло анафілактичних реакцій.
Аутоімунні антитіла
У контрольованих клінічних дослідженнях та за результатами постмаркетингового спостереження через рік встановлено, що 3,5 % пацієнтів, які отримували голімумаб, та 2,3 % пацієнтів контрольної групи стали позитивними за результатами тесту та антинуклеарні антитіла (ANA-позитивні) та мали титри 1:160 та вище. Частота появи антитіл до двоспіральної ДНК через рік була незначною.
Передозування Сімпоні розчин д/ін., 100 мг/мл по 0,5 мл у поперед. запов. руч. №1 з автоін`єкт.
У одному з клінічних досліджень вводилися одноразові дози до 10 мг/кг внутрішньовенно, при цьому дозообмежуючої токсичності не спостерігалося. При передозуванні рекомендується контроль стану пацієнта для виявлення можливих проявів або симптомів побічних реакцій та проведення негайної відповідної симптоматичної терапії
Застосування в період вагітності або годування груддю Сімпоні розчин д/ін., 100 мг/мл по 0,5 мл у поперед. запов. руч. №1 з автоін`єкт.
Жінки дітородного віку. Жінки дітородного віку мають використовувати адекватні методи контрацепції для попередження вагітності до, під час лікування та протягом 6 місяців після завершення лікування голімумабом.
Вагітність.
Дані щодо застосування голімумабу під час вагітності відсутні. Внаслідок пригнічення TNF, введення голімумабу підчас вагітності може впливати на імунну відповідь у новонародженого. В дослідженнях на тваринах не відмічалося прямих або опосередкованих ознак впливу на вагітність, розвиток ембріона/плоду, пологи чи постнатальний розвиток. Застосування голімумабу під час вагітності не рекомендоване. Застосування голімумабу можливе лише у випадку ретельної оцінки співвідношення користь/ризик.
Голімумаб проникає через плаценту. Після лікування матері TNF-блокаторами під час вагітності, антитіла виявлялися у сироватці немовлят до 6-місячного віку. Відповідно, ці немовлята можуть мати підвищений ризик розвитку інфекцій. Введення живих вакцин немовлятам, які в утробі матері підлягали впливу голімумабу, не рекомендується протягом 6 місяців після останньої інфузії матері голімумабу під час вагітності (див. розділи «Особливості застосування» та «Взаємодія з іншими лікарськими засобами та інші види взаємодій»).
Годування груддю.
Невідомо чи екскретується голімумаб у молоко людини, або абсорбується після прийому всередину. Жінки мають утримуватися від годування груддю під час та протягом 6 місяців після припинення лікування голімумабом.
Фертильність.
Дослідження фертильності у тварин на фоні введення голімумабу не проводилося. Дослідження фертильності з використанням аналогічних антитіл, що вибірково пригнічують функціональну активність TNF мишей, не виявили ефекту на фертильність.
Умови зберігання Сімпоні розчин д/ін., 100 мг/мл по 0,5 мл у поперед. запов. руч. №1 з автоін`єкт.
Зберігати в холодильнику (2-8 °C). Не заморожувати. Зберігати у недоступному для дітей місці. Зберігати у зовнішній упаковці для захисту від світла.
Термін придатності
2 роки.
Упаковка
0,5 мл розчину у попередньо наповненому шприці зі скла типу 1 з гумовим наконечником та голкою, вкритою ковпачком, з пристроєм для введення UltraSafe, по 1 або по 3 шприци в картонній коробці.
0,5 мл розчину у попередньо наповненому шприці зі скла типу 1 з гумовим наконечником та голкою, вкритою ковпачком, у ручці з автоін?єктором, по 1 або по 3 ручки в картонній коробці.
Категорія відпуску
За рецептом.
Реєстраційні дані Сімпоні розчин д/ін., 100 мг/мл по 0,5 мл у поперед. запов. руч. №1 з автоін`єкт.
Виробник: Бакстер Фармасьютикал/Сілаг АГ для "Джонсон & Джонсон, ТОВ", США/Швейцарія
Фарм. група: Імуносупресанти. Інгібітори фактору некрозу пухлин альфа (TNF-альфа).
Реєстрація: № UA/15841/01/01 від 04.07.2017. Наказ № 760 від 04.07.2017
МНН: Golimumab
Код АТХ:
(L) Протипухлинні лікарські засоби та імуномодулятори
(L04) Імунодепресанти
(L04A) Імунодепресанти (імуносупресанти)
(L04AB) Інгібітори фактору некрозу пухлин-альфа (tnf-alfa)
(L04AB06) Голімумаб
Дата оновлення информації: 05.02.2025 р.
© likiteka 2025
- Ремикейд пор. ліофіл. д/п конц. в/в 100 мг фл. №1, Янссен Байолоджикс Б.В./Сілаг АГ для "Джонсон & Джонсон, ТОВ" , Швейцарія/Нідерланди/Російська Федер
- Фламмегіс ліофіл. д/р-ну д/інф 100 мг фл. №1, Егіс, Фармацевтичний завод, ЗАТ, Угорщина
- Хуміра р-н д/ін. 40 мг/0,8 мл шприц, у компл. з серветками №1, Веттер Фарма-Фертігунг ГмбХ і Ко. КГ для "Еббві Біофармасьютікалз", Німеччина/Швейцарія
- Хуміра розчин д/ін. по 40 мг/0,8 мл у шпр. №2 з сервет., Веттер Фарма-Фертігунг ГмбХ і Ко. КГ для "Еббві Біофармасьютікалз", Німеччина/Швейцарія
- Хуміра р-н д/ін. 40 мг/0,8 мл фл., +шпр., голка, адаптер, 2 серв. №2, Веттер Фарма-Фертігунг ГмбХ і Ко. КГ для "Еббві Біофармасьютікалз", Німеччина/Швейцарія
- Енбрел р-н д/ін. 25 мг шприц 0,5 мл №4, Ваєт Фармасеутикалс для "Пфайзер Ейч. Сі. Пі. Корпорейшн" (Великобританія, США)
- Енбрел р-н д/ін. 50 мг шприц 1 мл №4, Ваєт Фармасеутикалс для "Пфайзер Ейч. Сі. Пі. Корпорейшн" (Великобританія, США)
- Енбрел Ліо пор. д/р-ну д/ін. 25 мг фл., з розч. у шприце №4, Ваєт Фармасеутикалс для "Пфайзер Ейч. Сі. Пі. Корпорейшн" (Великобританія, США)
- Хуміра розчин д/ін. по 40 мг/0,8 мл у шпр. №1 з сервет., Веттер Фарма-Фертігунг ГмбХ і Ко. КГ для "Еббві Біофармасьютікалз", Німеччина/Швейцарія
- Хуміра р-н д/ін. 40 мг/0,4 мл фл., +шпр., голка, адаптер, 2 серв. №2, Веттер Фарма-Фертігунг ГмбХ і Ко. КГ для "Еббві Біофармасьютікалз", Німеччина/Швейцарія
- Хайрімоз 40 розчин д/ін. по 40 мг/0,8 мл у шпр. по 0,8мл №2, Сандоз ГмбХ, Австрія
- Хуміра розчин д/ін. по 20 мг/0,2 мл у шпр. №2 з сервет., Веттер Фарма-Фертігунг ГмбХ і Ко. КГ для "Еббві Біофармасьютікалз", Німеччина/Швейцарія